Dr. Laxmaiah Manchikanti의 분석에 따르면, 매년 약 9백만 건의 ESI가 시행됩니다.
이 주사에 사용되는 코르티코스테로이드는 이 특정 목적에 대해 FDA 승인을 받지 않았습니다.
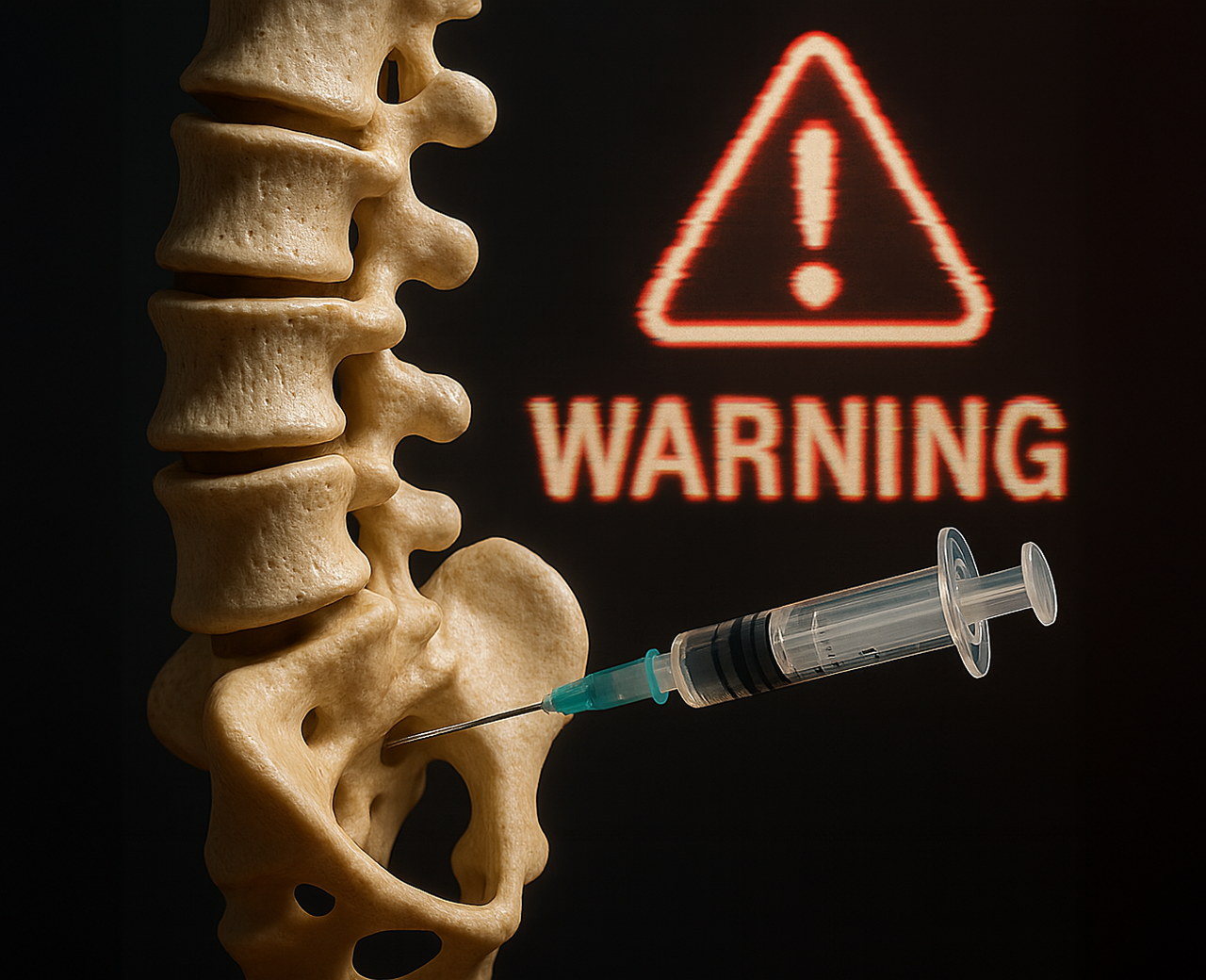
미국 식품의약국(FDA)은 허리와 목 통증에 사용되는
경막외 스테로이드 주사(ESI)에 대한 MedWatch Alert를 발표했습니다.
이 경고는 "척추의 경막외 공간에 코르티코스테로이드를 주사하는 것은
시력 상실, 뇌졸중, 마비, 사망을 포함한 드물지만 심각한 부작용을 초래할 수 있다"고
명시하고 있습니다.
ESI는 척수와 척추의 뼈 구조 사이에 위치한 경막외 공간에 코르티코스테로이드를 주사하는 시술입니다.
Dr. Laxmaiah Manchikanti의 분석에 따르면, 매년 약 9백만 건의 ESI가 시행됩니다.
이 주사에 사용되는 코르티코스테로이드는 이 특정 목적에 대해 FDA 승인을 받지 않았습니다.
FDA는 이제 메틸프레드니솔론, 하이드로코르티손, 트리암시놀론, 베타메타손, 덱사메타손을 포함한 주사형 코르티코스테로이드의 약물 라벨에 이러한 위험을 설명하는 경고를 추가하도록 의무화하고 있습니다.
이 새로운 경고는 스테로이드를 경막외 공간에 주사하는 것과 관련된 위험을 강조하는 것을 목표로 하지만, 가능한 모든 부작용을 열거하지는 않습니다.
현재 약물 라벨의 세부 사항에 명시된 이러한 부작용에는 "거미막염, 방광/장 기능 장애, 두통, 수막염, 하지 마비/하반신 마비, 발작, 감각 장애"가 포함됩니다.

2009년, FDA는 특정 유형의 경막외 스테로이드 주사의 안전성을 연구하기 위한 그룹을 소집했습니다. FDA는 이 그룹의 권고 사항이 아직 계류 중이며 완료되는 대로 발표될 것이라고 밝혔습니다.
ESI에 반대하는 그룹인 경막외 약물 미준수(EDNC)의 데니스 카폴롱고는 FDA의 새로운 경고가 "씁쓸하다"고 표현하며, 충분히 강력하지 않다고 시사했습니다. 카폴롱고는 FDA가 심각한 부작용이 "발생할 수 있다"고 단순히 명시하기보다는, 경막외 공간에서 이러한 스테로이드의 사용을 금지하는 더 강력한 지시를 내려야 한다고 주장합니다.

FDA의 현재 입장과 달리, 호주와 뉴질랜드의 보건 당국은 스테로이드가
"수막 내, 경막외, 정맥 내 또는 기타 불특정한 경로로 사용되어서는 안 된다"고
주장하는 더 강력한 성명을 발표했습니다.
남아프리카 공화국 정부도 유사한 경고를 발표한 것으로 알려졌습니다.
FDA가 이러한 절차에 대한 연구를 계속하고 있는 것은 기관의
추가적인 조치가 있을 수 있음을 시사합니다.
